
#脑海Yeah 第55期#吕薇
自古以来,从出生到衰老死亡,是生物发展的自然规律。古代有不少帝王,在权力巅峰时期,为了长生不老,求丹问药。
在现代文明飞速发展的今天,逆转衰老仍然是研究者们感兴趣的科学问题。60多年前,美国康奈尔大学采用一种听起来十分残酷的伤口愈合法,将一只年轻鼠和一只老年鼠的伤口缝合在一起,使它们建立血液循环共享系统。几个月之后,两只小鼠的骨骼在重量、体积和密度上竟然变得十分相似。后续的一系列实验证明,年轻鼠的血液可以改善老年鼠的肌肉状态以及记忆功能。
大脑作为智慧中枢,也抵挡不了岁月的摧残,大脑老化是痴呆和神经退行性疾病的基础,脑脊液作为脑细胞的直接生存环境,为大脑提供营养物质。既然血液当中存在这样的“置换反应”,那么对于大脑中直接为脑细胞提供生存与代谢环境的脑脊液,是否也存在这样的“年轻化”效应呢?Tony.W教授团队针对这一问题,进行了如下研究。
Part1 年轻脑脊液参与调节少突胶质细胞的增殖并改善老年鼠的记忆巩固
首先,研究者们对20月龄的老年小鼠进行与音调和灯光相关联的三次足部电击,并随机分成两组,分别连续注射人工脑脊液(aCSF)和年轻小鼠脑脊液(YM-CSF)7天,在第22天进行记忆测试,发现YM-CSF注射组的小鼠具有更好的记忆能力。随后,通过RNA 测序,检测年轻小鼠脑脊液注入对海马转录组的影响,发现少突胶质细胞相关基因高度上调,少突胶质前体细胞(OPC)的增殖和分化也明显增加,髓鞘水平上升。并且,在海马中注射年轻人类脑脊液可以得到相同的体内结果。同时,对体外培养的OPC进行上述两种脑脊液的处理,结果与体内试验结果相类似。
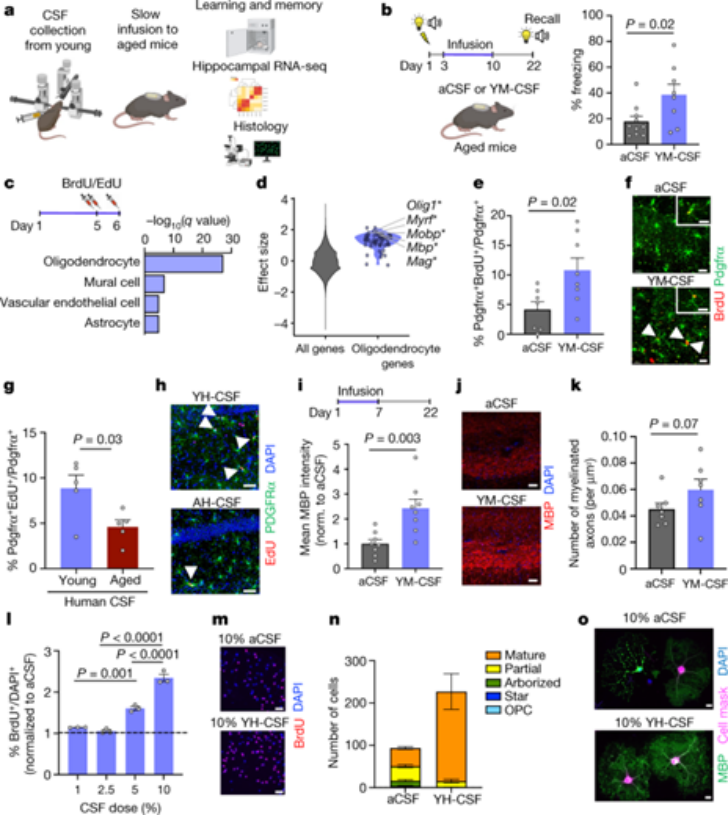
图 1:年轻YM/YH-CSF改善记忆巩固并促进OPC增殖分化。
Part2 血清应答因子(SRF)介导年轻脑脊液对OPCs的影响
为了探究年轻小鼠CSF如何诱导OPC的增殖分化,研究者们对培养的OPCs进行代谢RNA测序,经过一系列筛选,发现暴露于YH-CSF后1小时,OPC中SRF基因mRNA转录水平表达最高,暴露于YH-CSF后6小时后,SRF的靶向基因表达达到最高,且OPC的肌动蛋白细胞骨架密度增加,在YM-CSF注射组的小鼠中也得到类似的结果。在OPC敲除SRF之后,YH-CSF对OPC的影响消失,说明YM/YH-CSF对OPC的作用依赖于SRF。
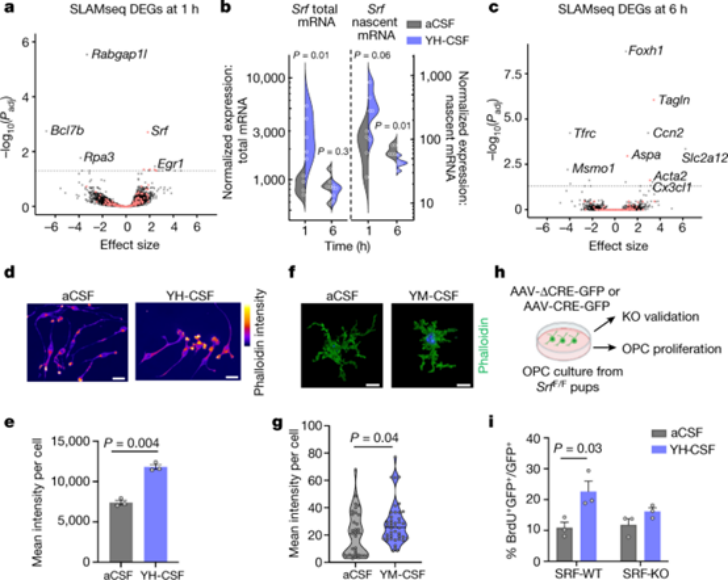
图2:SRF介导YM/YH-CSF对OPCs的影响
研究者发现在衰老小鼠海马CA1区,OPCs中SRF表达及其靶向基因的表达明显降低,且OPCs中关于细胞分化,细胞代谢以及蛋白质折叠的信号通路被抑制。在注射年轻CSF之后,老年鼠中SRF靶向基因的表达增加这些靶向基因参与重要的细胞活动,如GTPase酶活性调节、染色质组织、转录因子结合、细胞周期和细胞骨架组织调节。
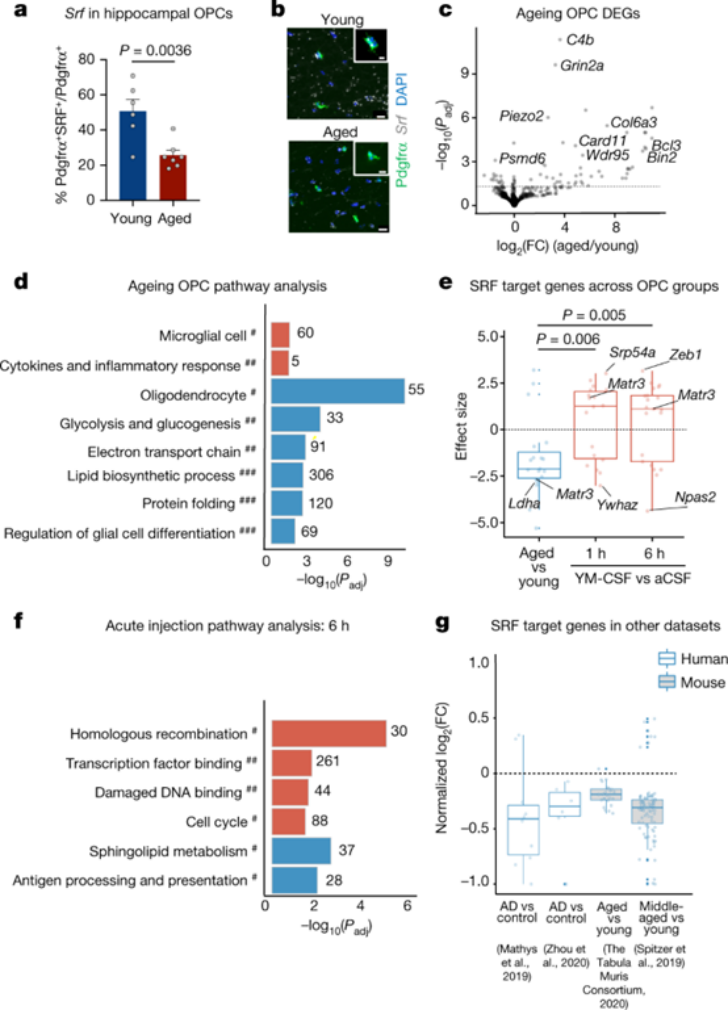
图3:海马OPC的SRF信号随衰老发生的下调能够被YM/YH-CSF诱导激活
Part3 CSF中Fgf17是影响OPCs和记忆的关键物质
CSF中含有数百种可能诱导SRF信号传导的蛋白质,研究者通过对比CFS蛋白质组数据库进行筛选分析,筛选出35种潜在的SRF诱导物质,为了测试这些候选物的活性,用SRE-GFP报告基因转染HEK293细胞,对SRF激活基因进行筛选,发现成纤维细胞生长因子Fgf17和Fgf8的效应最强,且呈剂量依赖。由于Fgf17在大脑中富集,因此研究者将目光锁定在Fgf17。Fgf17的水平在衰老人类的CSF、血液以及小鼠的神经元中有所降低,根据以往的研究,Fgf17通过激活Rho GTPase和调节肌动蛋白来激活SRF途径。
在原代培养的OPCs中,加入Fgf17可以促进OPCs增殖和分化,在老年小鼠中注射重组Fgf17,发现老年小鼠海马中的OPCs相比于对照组增殖明显,且老年小鼠记忆功能有所改善。
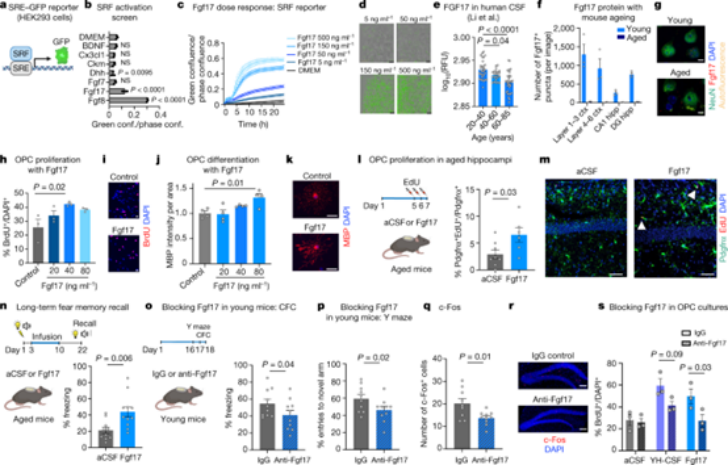
图4:Fgf17促进OPC增殖以及记忆改善
总结:这项研究发现年轻个体CSF通过上调Fgf17水平促进OPCs的增殖以及海马髓鞘形成,改善老年小鼠的记忆功能。这可能是预防或挽救与衰老和神经退行性疾病相关的认知衰退的一种策略。
 微信客服
微信客服
 微信公众号
微信公众号