16p11.2微缺失指基因组位置29.5-30.1Mb(BP4-BP5)之间发生的基因组拷贝数缺失,缺失长度约500kb。16p11.2区域两端都存在约147 Kb低拷贝重复序列(99.5%序列同源)导致基因组在复制过程中容易发生染色体间或者染色体内重组,形成CNVs。
16p11.2微缺失是儿童神经发育障碍(Neurodevelopmental disorders,NDDs)的重要遗传因素之一,影响了儿童身心健康,给社会、家庭带来一系列沉重负担。与其它典型致病性微缺失综合征不同的是,16p11.2微缺失携带者的神经发育表型存在显著差异,而其表型异质性的机理并不清楚,使得遗传学家无法开展遗传咨询和产前诊断。
近日,首都儿科研究所陈晓丽课题组在Brain杂志在线发表了题为Haplotype-specific MAPK3 expression in 16p11.2 deletion contributes to variable neurodevelopment 的研究论文。该工作发现剩余单体型不同使MAPK3基因差异表达进一步导致16p11.2微缺失神经细胞表型异质性。
首先研究者通过多中心协作联合建立了首个中国16p11.2微缺失神经发育障碍队列,分析了患儿的受累神经发育表型类型,其核心表型包括癫痫(61%)、智力障碍(48%)和孤独症谱系障碍(23%)。之后对携带者进行16p11.2区域全测序,分析了携带者的剩余16p11.2区域序列,未发现致病性或可能致病性编码突变,但发现包含58个SNP绝对连锁,形成132kb的不同单体型,分别为野生(H2,由58个野生SNP构成)和突变单体型(H1,由58个野生SNP构成)。
为了解不同剩余单体型和神经发育表型的可能关系,研究者选择了两个核心家系(家系中包含性别相同、剩余单体型和神经发育表型不同的2个携带者)建立了iPSCs系和神经细胞模型,发现16p11.2微缺失在神经元的发育早期影响基因组转录表达,在成熟神经元引起胞体增大、电生理活性增强;更重要的是,研究发现MAPK3基因是16p11.2微缺失相关神经发育障碍的重要贡献基因,且剩余单体型对MAPK3基因进行顺式表达调控(H1降低MAPK3表达,H2增加MAPK3表达),导致16p11.2微缺失神经细胞出现不同发育表型,之后采用工具细胞体外荧光报告实验证实剩余单体型通过10个增强子SNP调控MAPK3表达;最后研究者利用不同种族的3个16p11.2微缺失携带者队列(SFARI-ASD、CIP-NDD、PUMCH-CS)验证剩余单体型和儿童NDDs发生相关(H1增加儿童NDDs风险,H2降低儿童NDDs风险)。
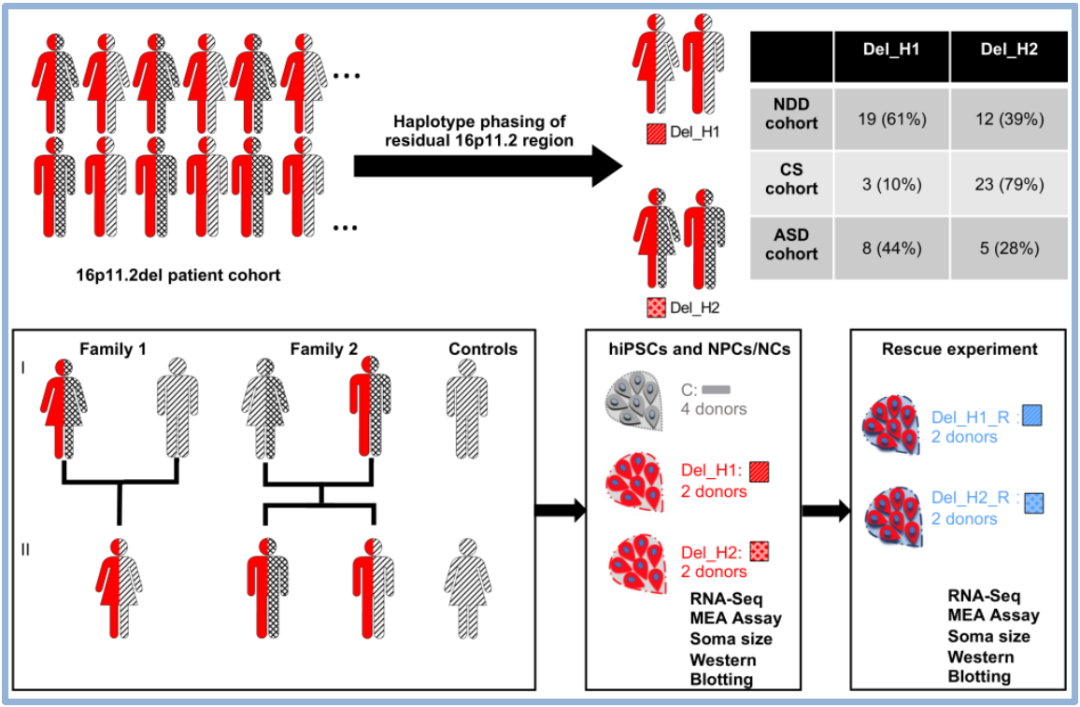
图1 研究思路
至此,该研究阐明了16p11.2微缺失神经发育表型异质性的其中一个机制,为今后研究16p11.2微缺失的肥胖、高脂血症、贫血的表型异质性提供思路,也为研究其他表型外显差异的基因组病(1q21.1 deletion,15q11.2 BP1-BP2 deletion,16p11.2 BP1-BP3 deletion,22q11.2 deletion)提供思路。
首都儿科研究所陈晓丽研究员团队的博士/硕士研究生刘芳、梁晨、李政昌和北京协和医院骨科赵森博士为本文共同第一作者。首都儿科研究所陈晓丽研究员为唯一通讯作者。
原文链接:https://doi.org/10.1093/brain/awad071
 微信客服
微信客服
 微信公众号
微信公众号