资讯分类导航:
微信扫一扫分享


文章来源:【公众号】自闭症医学进展;ID号:woniubbhealth
简介:今年一月份,美国哈佛医学院JunR.Huh团队发现了孤独症儿童常伴随免疫失调和胃肠道症状的可能原因,是由于母亲孕期的免疫激活和肠道菌群失调。并将他们的研究成果发表在Cell《细胞》杂志的子刊Immunity上。

1.研究背景
人在胎儿时期所接触到的环境因素对后续健康起到关键性影响。流行病学研究表明,多种神经发育障碍及炎症性、代谢性疾病的发生发展均与患者在生命早期接触到不良环境有关,如母亲于怀孕期间有过感染经历、母亲曾于孕期高脂饮食或营养不良等。
其中,多项研究提示孕期病毒感染易使后代增加患孤独症谱系障碍的风险。值得关注的是,ASD患者常伴随免疫功能及胃肠道功能失调,表现出多种炎症症状,如促炎细胞因子水平升高、淋巴结增生、小肠炎等。然而,炎症表现为何会作为神经发育障碍的共病症状还有待探索。
孤独症谱系障碍(ASD)是儿童的神经发育障碍,儿童常伴随免疫失调和胃肠道不适症状,但其机理尚不清楚。本项研究借由母体免疫激活(MIA)孤独症小鼠模型进行实验,提出了孤独症儿童易出现免疫失调和胃肠道症状的可能原因,并强调了母亲孕期肠道菌群在其中起到的关键性作用。
2.研究方法
1)孤独症及对照组小鼠模型
聚肌胞苷酸[poly(I:C)]是一种免疫增强剂。向怀孕母鼠注射聚肌胞苷酸,可激活母鼠的免疫应答,并造成后代小鼠出现社交障碍、刻板行为等ASD症状,是目前常用的一种构建ASD小鼠模型的方法。这种ASD小鼠又被称为母体免疫激活仔鼠,或MIA仔鼠。
磷酸盐缓冲生理盐水(PBS)具有和体液相近的渗透压和酸碱度。母鼠怀孕期间注射PBS不会对仔鼠造成影响,故将其后代作为MIA仔鼠的对照组,被称为PBS仔鼠。
2)细菌诱导的小鼠肠炎模型
鼠类柠檬酸杆菌常用于构建小鼠结肠炎和黏膜免疫应答模型。本研究通过给仔鼠口服该菌,使仔鼠出现细菌感染导致的肠道炎症。为使肠炎表型更加稳定,仔鼠在口服该菌之前须首先服用甲硝唑,以避免厌氧菌造成影响。

3.研究成果
1)孤独症小鼠对细菌感染引发的肠道炎症的易感性增强(免疫致敏)
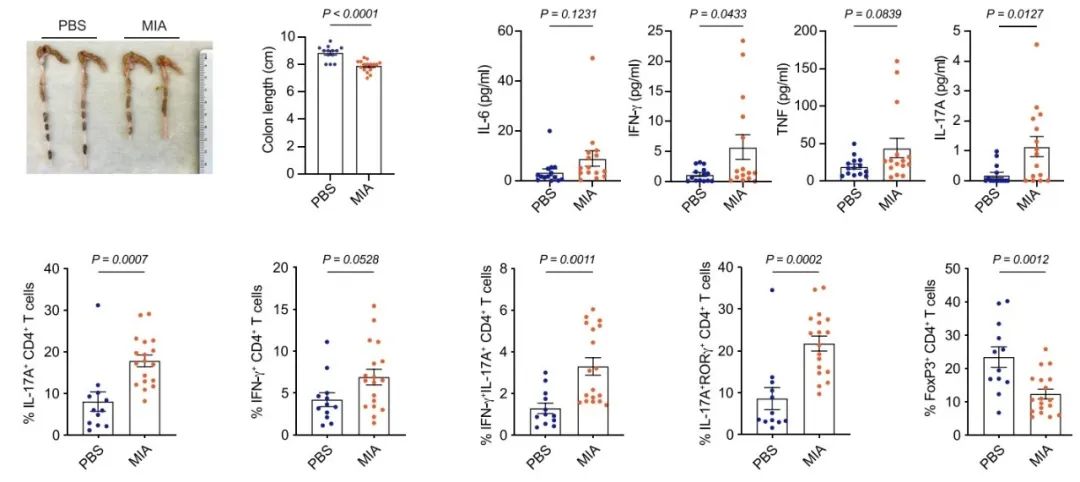
研究发现,MIA仔鼠和PBS仔鼠在感染鼠类柠檬酸杆菌前各项指标无明显差异。但二者在感染鼠类柠檬酸杆菌之后,MIA仔鼠出现更明显的肠道病变,其结肠长度显著短于PBS仔鼠。
CD4+T细胞在获得性免疫应答中起重要作用,部分CD4+T细胞可分泌促炎细胞因子白细胞介素-17A(IL-17A)。在感染鼠类柠檬酸杆菌后,MIA仔鼠血清中IL-17A的水平以及结肠中表达IL-17A的CD4+T细胞(IL-17A+CD4+T细胞)的占比均显著高于PBS仔鼠。
上述结果提示,母体免疫激活不仅可使小鼠出现ASD症状,还会使小鼠增强对细菌感染引发的肠道炎症的免疫应答,即免疫致敏,并使小鼠肠道出现显著的病理性改变。
研究人员进一步发现IL-17A在母鼠孕期免疫激活与仔鼠免疫致敏之间起到桥梁性作用。他们先给孕鼠注射IL-17A的抗体再向其注射聚肌胞苷酸,使孕鼠免疫激活但血清中的IL-17A失去免疫效应。这种孕鼠被称为“抗IL-17AMIA母鼠”。发现后代小鼠的结肠长度以及结肠中IL-17A+CD4+T细胞的占比与PBS对照组相比均无显著差异,即免疫致敏现象消失。这提示孕期免疫激活引发母鼠血清中IL-17A水平升高可能是导致仔鼠出现免疫致敏的原因。

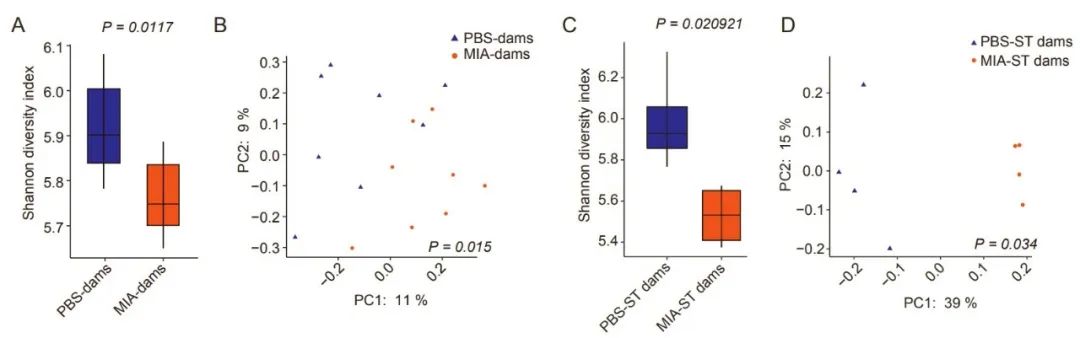
2)因免疫激活造成母鼠肠道菌群组成变化使小鼠出现免疫致敏
研究人员发现MIA母鼠的肠道菌群α多样性和β多样性均显著低于PBS母鼠,提示免疫激活会影响母鼠肠道菌群。为探究母鼠肠道菌群在母体免疫激活引发小鼠免疫致敏过程中的可能作用,研究人员在无菌小鼠肠道中单一定植分节丝状菌(SFB),该菌可促使CD4+T细胞分泌IL-17A。这样可使小鼠肠道在缺乏肠道菌群的情况下过表达IL-17A。在小鼠怀孕期间向其注射聚肌胞苷酸使其免疫激活(或注射PBS作为对照)。
实验结果表明单一定植SFB的MIA仔鼠出现了社交障碍和刻板行为,但用鼠类柠檬酸杆菌进行感染并未出现结肠长度明显缩短,和结肠中IL-17A+CD4+T细胞占比显著增加的情况。说明缺乏肠道菌群的母鼠在免疫激活后所生小鼠未出现免疫致敏现象,提示母体肠道菌群在母体免疫激活引发后代免疫致敏过程中起到不可或缺的作用。
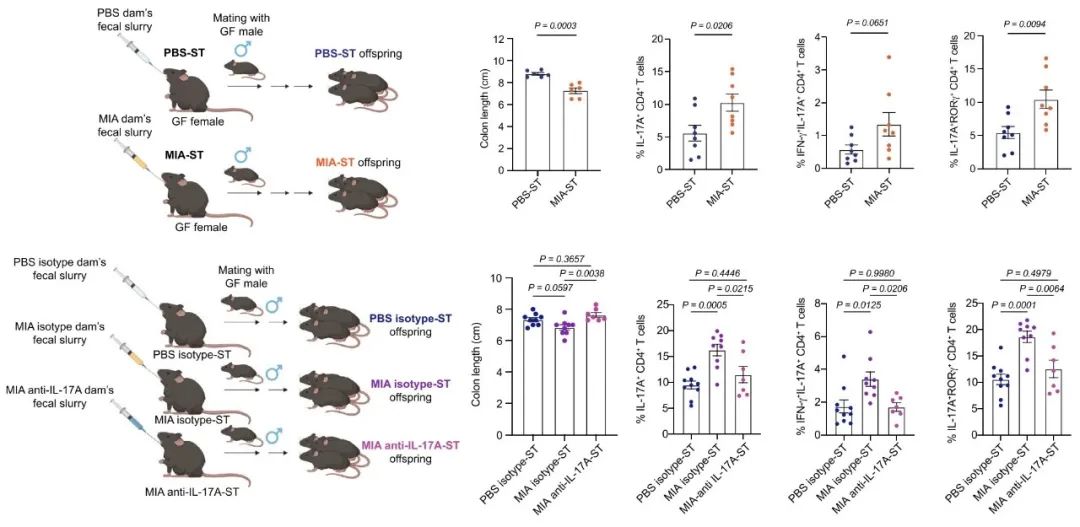
为进一步探究肠道菌群的作用机制,研究人员分别将PBS母鼠、MIA母鼠、抗IL-17AMIA母鼠的粪菌移植给无菌母鼠,再让无菌公鼠分别与上述经粪菌移植后的母鼠交配,所生后代称为PBS-ST仔鼠、MIA-ST仔鼠和抗IL-17AMIA-ST仔鼠。再将这些仔鼠用鼠类柠檬酸杆菌进行感染。
结果表明,在感染鼠类柠檬酸杆菌后,MIA-ST仔鼠出现了与MIA仔鼠近似的免疫致敏现象,包括结肠长度较PBS-ST仔鼠明显缩短,结肠中IL-17A+CD4+T细胞占比较PBS-ST仔鼠明显升高;同时,抗IL-17AMIA-ST仔鼠也出现了与抗IL-17AMIA母鼠相近的免疫致敏消失现象,其结肠长度以及结肠中IL-17A+CD4+T细胞的占比与PBS对照组相比均无显著差异。这说明,母体免疫激活通过使IL-17A的免疫效应增强,造成肠道菌群组成改变,导致后代出现免疫致敏现象,即对细菌感染引发的肠道炎症的易感性增强。

3)母鼠免疫激活使小鼠获得性免疫应答功能增强进而出现免疫致敏
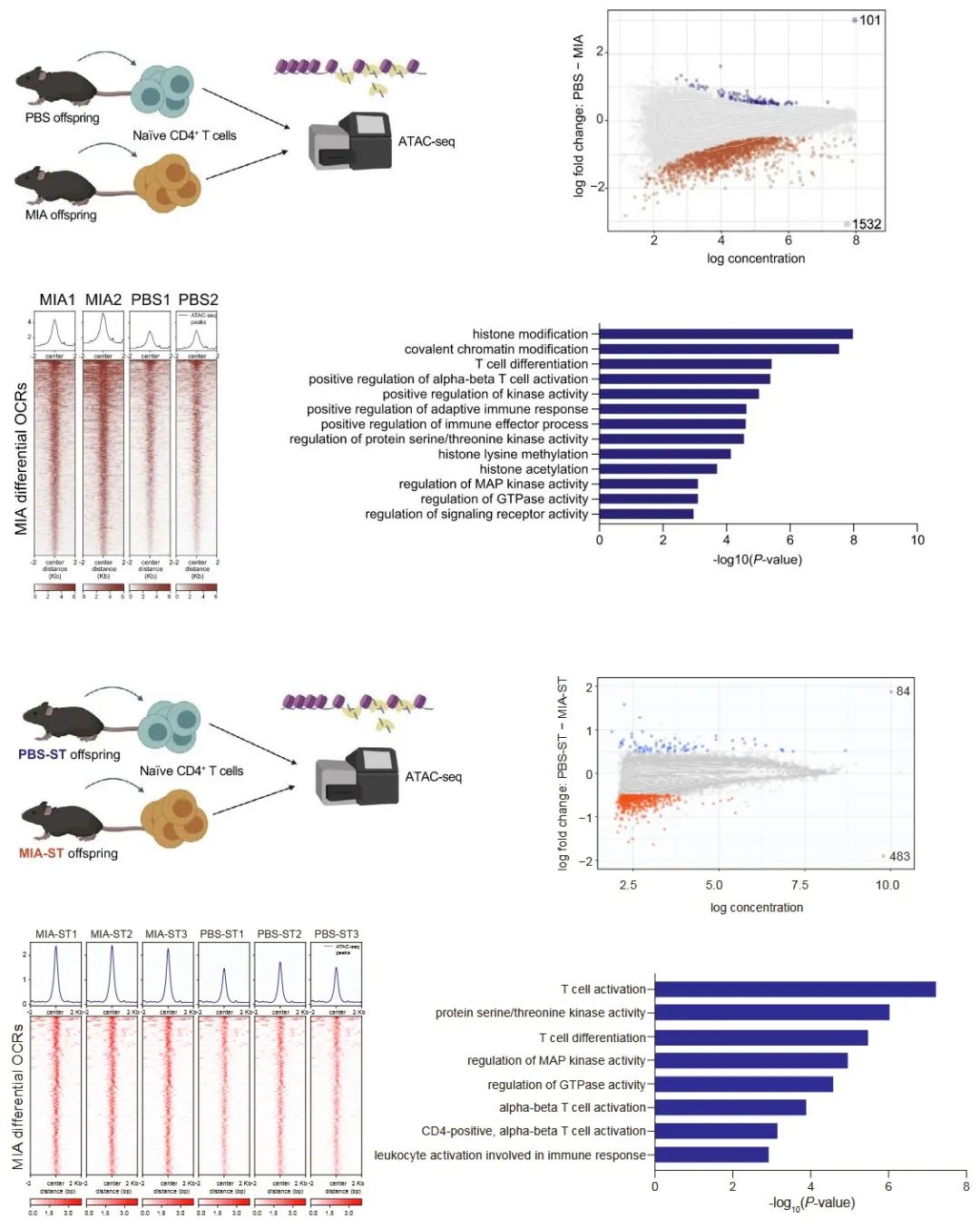
MIA仔鼠和MIA-ST仔鼠的核心免疫致敏表现为结肠中IL-17A+CD4+T细胞的比例升高,及其所导致的血清IL-17A水平升高,而该现象的出现表明这两种仔鼠在细菌感染后结肠中CD4+T细胞中相关基因的表达水平异常升高,提示这两种母体免疫激活仔鼠可能在细菌感染前其CD4+T细胞就已存在异常。研究人员对MIA和MIA-ST仔鼠脾脏和淋巴结中的初始CD4+T细胞进行高通量测序,发现有成百上千种与获得性免疫应答增强、染色质修饰与重塑等功能相关的基因高表达。
上述结果提示,母体免疫激活(包括肠道菌群异常导致的母体免疫激活)使后代的CD4+T细胞的染色质开放程度增加,导致后代的获得性免疫应答功能增强,使后代在细菌感染时的炎症反应增强。
4.结论
本项研究通过对母体免疫激活孤独症小鼠模型进行实验,阐释了孤独症儿童常伴随免疫失调和胃肠道症状的可能原因:
母亲在怀孕期间因感染等原因造成免疫激活可能造成孩子出生后出现神经发育障碍,即孤独症。同时,免疫激活还会增强母亲体内IL-17A的免疫效应并影响肠道菌群组成,二者一并造成孩子出生后CD4+T细胞的染色质开放性增加,使孩子的获得性免疫应答功能增强。导致孩子在因受到细菌感染等原因出现肠道炎症时,肠道中IL-17A+CD4+T细胞比例及血清中IL-17A水平过度升高,造成炎症反应增强(即免疫致敏),进而易出现胃肠道不适等症状。
此外,肠道菌群失调自身也可增强孕妇体内IL-17A的免疫效应,进而使孩子出现免疫致敏及胃肠道不适。
综合上述结论,孕期避免感染和炎症,同时保持健康的肠道菌群,有助于避免孩子出现孤独症以及由免疫致敏引发的长期胃肠道不适症状。

综上,本项研究发现母亲孕期出现炎症易导致后代出现免疫系统功能失调,使后代在因各种因素出现炎症时炎症反应更为强烈。这阐释了神经发育障碍患者常伴随各种炎症症状的可能原因,即孤独症患者炎症表现增强可能是由于其母亲在怀孕期间炎症水平较高。本项研究还发现母亲的肠道微生物组与后代神经系统发育和免疫系统发育之间具有联系,有助于理解和进一步探究母亲孕期微生物感染对孩子造成的长期影响。
参考文献:
Kim E, et al. Maternal gut bacteria drive intestinal inflammation in offspring with neurodevelopmental disorders by altering the chromatin landscape of CD4+ T cells. Immunity, 2022; 55(1):145-158.
doi: 10.1016/j.immuni.2021.11.005






2022-06-09
2020-09-05
2020-09-05
2021-04-22
2021-08-15
2025-05-23
2025-11-05


2023-05-14
2022-07-18
2020-05-11
2025-05-13
2025-05-12
2025-05-13
2024-05-17
2026-05-11


2023-08-31
2024-08-22
2024-01-07
2023-07-14
2023-04-04
2024-09-06
2023-08-12
2023-05-09
2023-05-04
2023-05-11
扫码拨打
微信客服
 微信客服
微信客服
微信公众号
 微信公众号
微信公众号






















