
肠屏障通透性增加可通过激活脂多糖介导的Toll样受体4/髓样分化因子88/核因子kappa B信号通路介导孤独症的发生
Leaky Gut Plays a Critical Role in the Pathophysiology of Autism in Mice by Activating the Lipopolysaccharide-Mediated Toll-Like Receptor 4–Myeloid Differentiation Factor 88–Nuclear Factor Kappa B Signaling Pathway
李芳1 • 柯浩然2 • 王斯琪3 • 毛苇1 • 符策雄4 • 邓文林5
1海南医学院附属海南省人民医院消化内镜中心,海口570311,中国
2南方医科大学附属南方医院感染内科,广州510515,中国
3广州医科大学附属第一医院消化内科,广州510120,中国
4海南省人民医院肝胆外科,海口570311,中国
5中山大学附属第六医院儿科,广州510655,中国
第一作者:李芳、柯浩然、王斯琪、毛伟、符策雄
通讯作者:邓文林
孤独症谱系障碍(ASD),是一组病因未明,以社交困难和重复刻板行为为主要特征等神经系统性疾病,与身体的多个系统有关,包括神经系统、免疫系统和胃肠道等。在过去的几十年里,自闭症的患病率有急剧上升趋势。近年来,肠屏障功能正受到越来越多的关注。研究表明,孤独症儿童出现胃肠道症状的频率是正常儿童的4.4倍,临床症状主要包括便秘、腹泻和腹痛等。肠屏障通透性的增加可导致内毒素(脂多糖)移位,随后通过破损的肠屏障入血,再经血液循环透过血脑屏障最后进入颅内,激活一系列免疫反应进而影响大脑认知、行为功能,所谓的“肠-脑”轴的概念。
在本研究中,研究人员使用葡聚糖硫酸钠(DSS)和二甲双胍分别作为干预BTBR T+tf/J自闭症小鼠肠道屏障破坏和修复的诱导剂。研究结果显示,DSS介导的肠屏障破坏可导致三箱实验中孤独症小鼠的社交能力显著下降,与空笼子玩耍的时间比陌生小鼠更长。然而,给予二甲双胍修复BTBR T+tf/J小鼠肠屏障后,孤独症小鼠的社交能力可得到明显改善。因此,在肠屏障修复后,孤独症小鼠的重复性刻板行为减少,社会记忆力也得到相应的提高。
接着,研究人员对背后的分子机制进行了探索,认为与颅内脂多糖(LPS)介导的toll样受体4 (TLR4)/髓样分化因子88(MyD88)/核因子κB (NF-κB)信号通路的激活或抑制密切相关。研究结果显示,DSS诱导下,孤独症小鼠血清中LPS明显升高,大脑皮层TLR4/MyD88/NF-κB通路关键分子及其下游炎症因子表达水平被激活;相应的,二甲双胍干预后,血清中LPS浓度下降,此通路的关键分子及其下游炎症因子表达水平受到抑制。
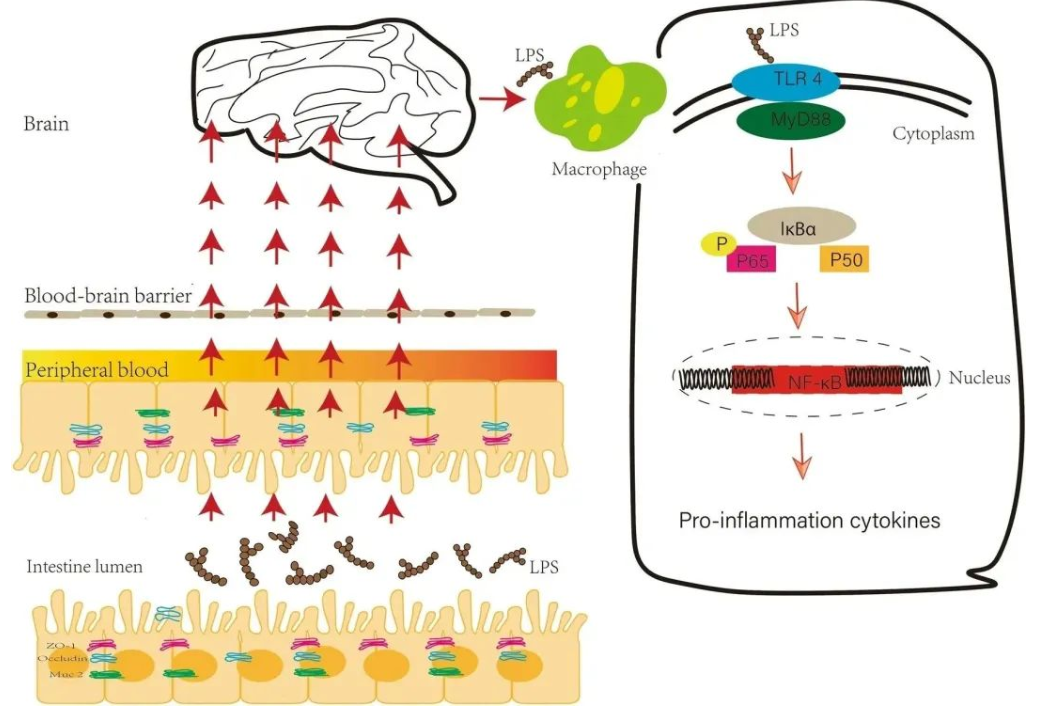
图1 内毒素导致自闭症谱系障碍的核心机制。“肠漏”可能会使肠道内毒素移位至脑组织,激活TLR4/MyD88/NF-κB炎症信号通路促进颅内炎症和神经退行性变的发生,导致自闭症症状。
综上所述,“肠漏”可能是孤独症发生的一个触发因素,其激活大脑皮层LPS介导的TLR4/MyD88/NF-κB通路可能是导致孤独症发生的重要分子机制。
 微信客服
微信客服
 微信公众号
微信公众号