孤独症谱系障碍(Autism spectrum disorder, ASD)是一种多因素导致、异质性高的神经发育障碍疾病,其特点为患儿社交沟通障碍和重复刻板行为,其中社交功能障碍(Social dysfunction)是ASD最主要的症状。尽早发现和治疗对于改善ASD患者预后至关重要。目前的治疗以康复训练为主,仍然缺乏有效治疗药物。因此,揭示ASD社交功能障碍的分子机制,对于找到具有潜在治疗价值的分子靶点具有更重要意义。
4月20日,空军军医大学基础医学院武胜昔/王亚周团队在EMBO Molecular Medicine杂志上发表题为“Axin2 coupled excessive Wnt-glycolysis signaling mediates social defect in autism spectrum disorders”的研究成果。
该研究团队通过使用两种广泛采用的ASD小鼠模型(Shank3-/-和VPA处理小鼠)及其相应的人类神经元,利用病毒或CRISPR-Cas9介导的基因调控、质谱分析及转录组学、突触功能和结构分析、分子生物学、细胞代谢调控等技术对上述两种ASD模型社交功能障碍的分子机制进行了一系列探索,尝试为其治疗提供潜在且新颖的分子靶点。

作者发现:遗传因素致ASD的 Shank3-/-小鼠和环境因素致ASD的丙戊酸(VPA)处理小鼠的前扣带回皮质(Anterior cingulate cortex, ACC,一个调控社交功能的关键脑区)中经典Wnt信号的异常激活、糖酵解水平异常升高。在野生型小鼠ACC中过度激活经典Wnt信号可引起糖酵解异常和社交障碍。另外,抑制上述两种ASD小鼠糖酵解可部分挽救突触表型和社交功能。
进而,作者发现上述两种ASD小鼠在出生后两周左右,ACC内Wnt信号和糖酵解水平开始上调并维持到成年。通常认为,经典Wnt信号在胚胎期高度表达,而出生后逐渐减弱。神经前体细胞主要依靠糖酵解供能,而成熟神经元更倾向于氧化磷酸化。
本研究结果表明ASD神经元胞内部分信号或代谢特征可能处于“未成熟状态”,从而其突触发育和突触功能可能受到影响,进而导致社交障碍。
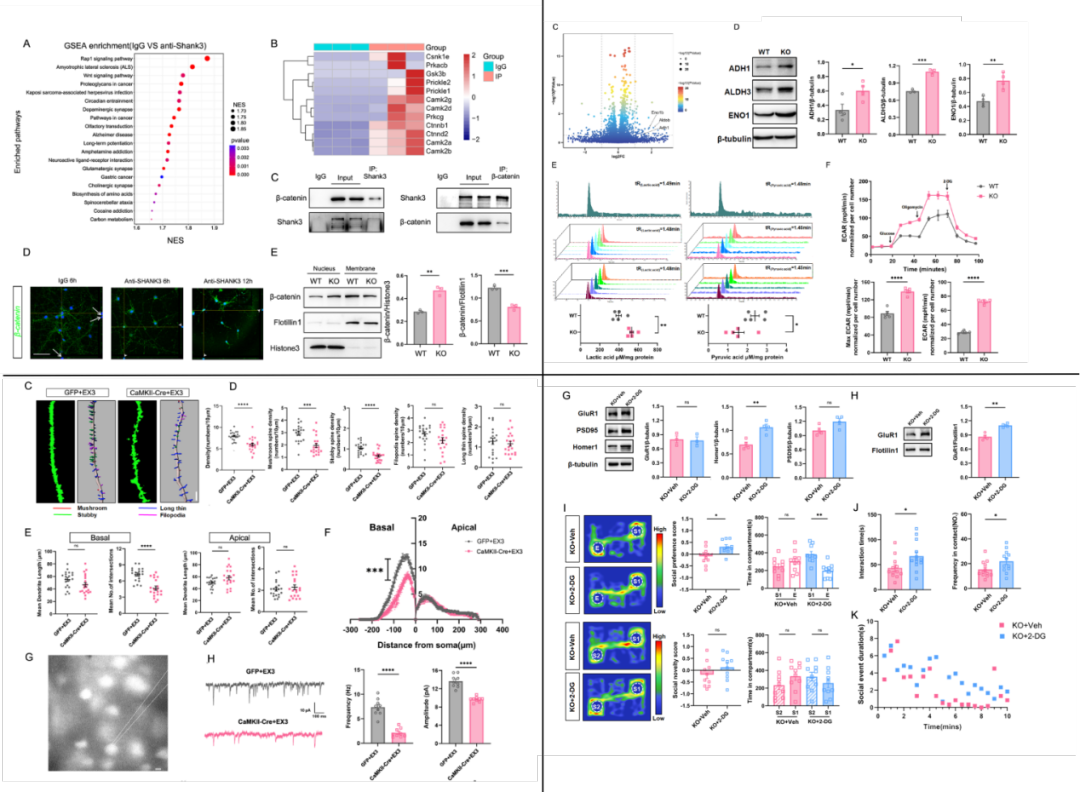
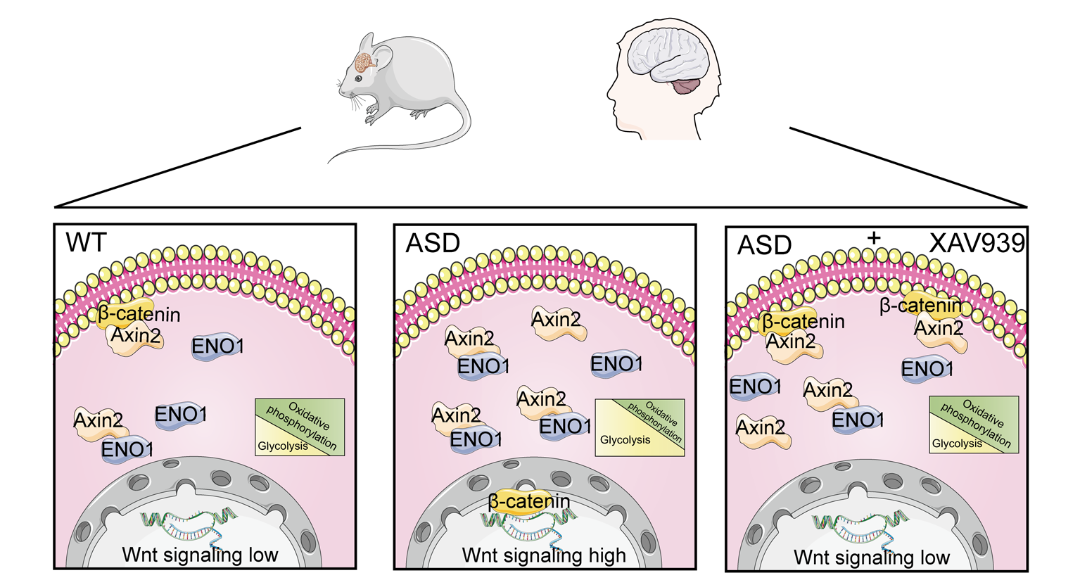
ASD神经元中Wnt信号与糖酵解之间是否存在交互作用?作者发现:在ASD神经元中,Axin2(一个Wnt信号通路中的反馈性抑制分子)与糖酵解途径的烯醇化酶(ENO1)相互结合显著增强,从而激活糖酵解。值得一提的是,本研究发现Axin2稳定剂XAV939可有效阻断胞浆内Axin2/ENO1的相互作用,同时抑制Wnt信号和糖酵解,将ASD神经元能量供应的重心从糖酵解转移到氧化磷酸化,从而促进突触成熟,使突触的表型和功能明显恢复,并有效改善两种ASD小鼠的社交障碍。
最后,作者进一步采用Shank3突变的人类胚胎干细胞和VPA预处理人类神经前体细胞,将其诱导为神经元后,观察了Wnt信号和糖酵解代谢。结果发现:在Shank3突变和VPA预处理的人神经元中,Wnt信号和糖酵解活性都异常升高。Axin2和ENO1在人ASD神经元中的互作也明显增强,XAV939处理可有效恢复人ASD神经元内Wnt-糖酵解信号水平和突触蛋白的表达。
随着众多的ASD风险基因和高危环境因素的不断发现,阐明ASD社交障碍的共性分子机制对于ASD药物开发具有重要意义。前人的临床遗传筛查研究提示Wnt信号可能是多种ASD风险基因的一个枢纽信号。临床生化分析也报道了大约30%的ASD患者存在代谢异常(不同研究组的数据可能有不同)。
本课题组应用两种经典的ASD模型及其人类神经元,首次报道了神经元内异常激活的Wnt -糖酵解信号是ASD突触缺陷和社交功能障碍的一个重要机制,提示Axin2作为ASD神经元中Wnt信号和糖酵解的汇合点,可作为改善ASD社交功能障碍的潜在治疗靶点。
空军军医大学武胜昔教授是文章的通讯作者,王亚周教授为共同通讯作者。文章的第一作者为王梦梦博士、共同第一作者为鲜盼盼博士和郑威安硕士。该研究得到中国科技创新2030-脑科学与类脑研究重大项目、国家自然科学基金创新群体项目、国家自然科学基金重点项目、陕西省重点研发项目等课题的支持。
原文链接:https://www.embopress.org/doi/full/10.15252/emmm.202217101
 微信客服
微信客服
 微信公众号
微信公众号