我们,基于神经科学的神经逻辑,而非心理学的归因和分析理论,并且将新的神经科学见解转化为实用的干预方法,努力实现孤独症干预的治疗效果最大化!
我们,基于大脑皮层发育的时间、前后和模态梯度,拥有从幼儿期靶向成年期的孤独症干预技术。
孤独症谱系障碍在临床上具有异质性,一些受影响的个体表现出轻微的(如果有的话)困难,而另一些人则经历非常痛苦的症状和一系列影响身心健康的同时发生的状况。
罕见或从头的高影响遗传变异通常具有诊断价值,通常在少于20%的孤独症个体中被确定,且常常在那些具有更复杂的医学表现的个体中。
多伦多儿童医院应用基因组学中心的研究人员在迄今为止最大规模的孤独症全基因组测序分析中,发现了与孤独症谱系障碍(ASD)相关的新基因和基因变化,使人们更好地理解了这种障碍背后的“基因组结构”。

这项研究昨天发表在《Cell》杂志上。研究人员使用全基因组测序(WGS)检测了来自Autism Speaks MSSNG (n=11,312)和Simons Simplex Collection (SSC; n=9,205) 的7000多名孤独症患者以及另外13000名兄弟姐妹和家庭成员的各种各样的基因变异。
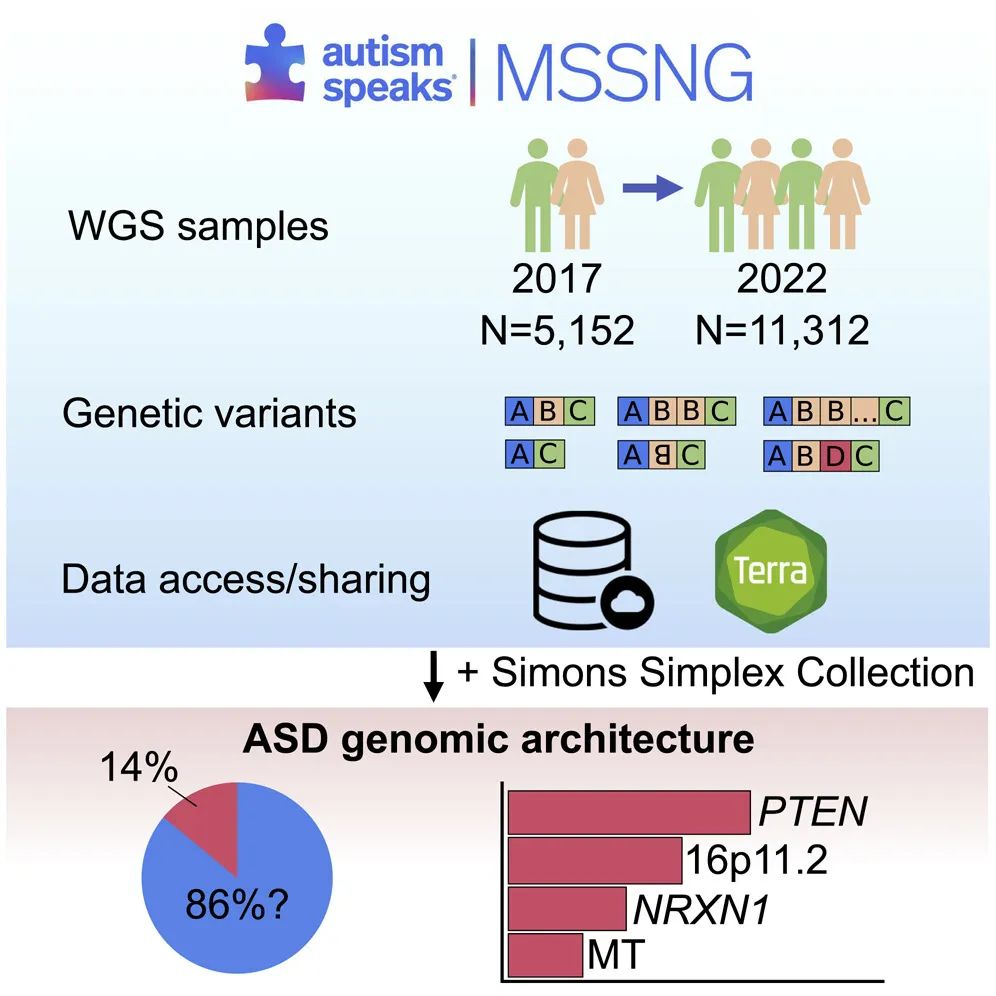
研究人员在来自MSSNG的718孤独症患者 (总数为5,100,占比为14.1%) 和来自SSC的350孤独症患者 (总数为2,419,占比为 14.5%) 中发现了与孤独症相关的134个罕见变异。考虑到基因组结构,52%为核序列级变异,46%为核结构变异(包括拷贝数变异、倒置、大插入、单亲源同二体和串联重复扩增),2%为线粒体变异。这项研究为探索携带与孤独症相关罕见变异的家庭的基因型-表型相关性提供了指南,并为进一步剖析剩下的~85%的特发性孤独症人口的病因研究提供了切入点。
该研究通过对所有参与者的整个基因组进行测序,并让参与MSSNG的家庭深度参与,将发现变异基因的潜力最大化,并分析包括所有类型的变异,从最小的DNA变化到影响整个染色体的变异。
该研究还指出了只有一个孤独症患者的家庭与有多个孤独症患者的家庭(即多发家庭)在孤独症遗传方面的重要细微差别。让研究小组感到惊讶的是,“多基因得分”—— 一种通过汇总整个基因组中数千种常见变异的影响来计算个体患有孤独症的可能性的估计—— 在多发家庭中并不高。
然而,应该强调的是,目前的所有研究仍然没有检查每一种可能的基因贡献。在一些已发表和正在进行的研究中,各种数据正被用于体细胞和表观遗传的研究,分别只占孤独症病例(样本数)的3-5%和1%。表观遗传的作用可能与发育过程中的特定基因组变异、环境暴露和/或(随机)变异有关。
人类基因组中只有2%是编码序列,98%属于非编码序列,所以DNA导致孤独症的变异可能并不全归因于基因。研究人员正试图深入研究剩下的98%的基因组,以寻找与孤独症相关的异常情况。到目前为止,对这些区域的了解还很少,但一些证据表明,孤独症与含有控制基因表达的调节元件的非编码DNA片段的变异有关。
随着在孤独症精准医疗应用中越来越强调基因-表型相关性、以及利用神经科学关于孤独症大脑的详细信息,个体层面的理解将是更早诊断和更好干预效果的关键,并可能最终为药理干预提供详尽的信息。
 微信客服
微信客服
 微信公众号
微信公众号